Stereokimia
adalah susunan ruang dari atom dan gugus fungsi dalam molekul umumnya
molekul organik dalam obyek tiga dimensi yang merupakan hasil hibridisasi dan ikatan secara geometri dari atom dalam molekul. Artinya bagaimana atom-atom dalam sebuah molekul diatur dalam ruang satu terhadap ruang yang lainnya.
molekul organik dalam obyek tiga dimensi yang merupakan hasil hibridisasi dan ikatan secara geometri dari atom dalam molekul. Artinya bagaimana atom-atom dalam sebuah molekul diatur dalam ruang satu terhadap ruang yang lainnya.
Isomeri
adalah gejala atau peristiwa terdapatnya beberapa senyawa berbeda yang
mempunyai rumus molekul sama. Senyawa-senyawa yang berisomeri dikatakan
merupakan isomer satu sama lain. Fenomena terdapatnya tiga senyawa berbeda,
yaitu 1-butanol (CH3 - CH2 - CH2 - CH2
- OH), 2-butanol (CH3 – CH – OH - CH2 - CH3)
dan dietileter (CH3 - CH2 – O - CH2 - CH3)
yang mempunyai rumus molekul sama, yaitu C4H9O, merupakan
gejala isomeri.
Senyawa 1-butanol merupakan isomer
dari senyawa 2-butanol, senyawa 1-butanol juga merupakan isomer dari senyawa
dietileter. Apakah 2-butanol merupakan isomer dari dietil eter? Tentu iya,
senyawa 1-butanol, 2-butanol dan dietileter merupakan isomer satu sama lain.
Oleh karena itu, isomer adalah suatu senyawa dari beberapa senyawa yang
mempunyai rumus molekul sama, tetapi mempunyai sifat berbeda akibat perbedaan
susunan atom-atomnya.
Dengan kata lain, isomer adalah suatu senyawa dari beberapa
senyawa berbeda yang mempunyai rumus molekul sama. Kata isomer berasal
dari kata Latin isomeres yang berarti mempunyai bagian yang sama. Isomeres
sendiri merupakan gabungan dari kata iso yang artinya sama, dan meros
yang artinya adalah bagian.
Perhatikan dua
senyawa berikut:
Kedua senyawa tersebut jelas
merupakan senyawa yang berbeda, hal tersebut diketahui dari struktur dan sifat
kedua senyawa yang berbeda. Senyawa 1-butena merupakan senyawa dengan rantai
karbon terbuka dan mempunyai gugus fungsi berupa ikatan rangkap dua, sedangkan
siklobutana merupakan senyawa dengan rantai karbon tertutup atau siklis dan
tidak mempunyai ikatan rangkap dua. Senyawa 1-butena berwujud gas pada suhu
kamar, karena mempunyai titik didih- 5oC, sedangkan siklobutana berwujud gas,
atau dapat berupa cairan pada daerah bersuhu rendah (yaitu yang mempunyai suhu
kamar kurang dari 13oC). Senyawa 1- butena mempunyai rumus molekul C4H8,
dan siklobutana juga mempunyai rumus molekul sama, C4H8. Karena
kedua senyawa merupakan senyawa berbeda tetapi mempunyai rumus molekul sama,
maka 1-butena dan siklobutana berisomeri.
Adakah senyawa lain selain 1-butena
dan siklobutana yang mempunyai rumus molekul C4H8? Apakah
2-butena merupakan isomer dari 1-butena dan siklobutana? Struktur 2-butena
adalah CH3CH = CHCH3. Senyawa ini berbeda dengan 1-butena
karena letak ikatan rangkap duanya berbeda, dan berbeda dengan siklobutana
karena rantai karbonnya terbuka, sedangkan siklobutana tertutup. Akan tetapi,
2-butena mempunyai rumus molekul yang sama dengan 1-butena atau siklobutana,
yaitu C4H8. Dengan demikian 2-butena adalah isomer dari
1- butena dan siklobutana.
Dapatkah Anda menemukan isomer lain
yang mempunyai rumus molekul C4H8? Bila jawaban Anda ya, tunjukkan struktur dan
nama dari isomer-isomer tersebut ? Dengan demikian, terdapat berapa isomer yang
mempunyai rumus molekul C4H8 ? Akan tetapi, bila jawaban Anda tidak terdapat
senyawa lain yang mempunyai rumus molekul C4H8, selain 1-butena, 2-butena, dan
siklobutana, pertimbangkanlah beberapa senyawa berikut:
Bila diperhatikan lebih lanjut,
ternyata terdapat dua jenis 2-butena, yaitu :
Cis-2-butena dan trans-2-butena
berbeda dalam susunan gugus atau atom yang terikat pada karbon ikatan rangkap,
pada cis-2-butena gugus-gugus metil terikat pada sisi ikatan rangkap yang sama,
sedangkan pada trans-2-butena gugus-gugus metil terikat pada sisi ikatan
rangkap yang bersebrangan. Perbedaan struktur keduanya menyebabkan sifat
keduanya juga berbeda, salah satunya dapat ditunjukkan dari titik didih
cis-2-butena dan trans-2-butena yang berbeda. Dengan demikian, cis-2- butena
dan trans 2-butena merupakan isomer satu sama lain.
Suatu molekul dapat bergerak dalam
ruang, menekuk atau membelit sehingga dapat digambarkan dengan beberapa cara
yang berbeda. Oleh karena itu, perlu kehati-hatian untuk menentukan apakah
suatu struktur merupakan isomer dari struktur yang lain, atau merupakan senyawa
yang identik. Perhatikanlah struktur-struktur di bawah ini, setiap baris
struktur yang ditunjukkan bukan merupakan isomeri, tetapi merupakan senyawa
identik.
Jenis-jenis
Isomeri
Senyawa-senyawa yang berisomeri
adalah senyawa-senyawa yang berbeda satu sama lain, dan perbedaannya disebabkan
oleh cara penyusunan atom-atomnya. Terdapat dua jenis isomeri, yaitu isomeri struktur dan stereoisomeri. Isomeri struktur adalah isomeri dengan
perbedaan terletak pada urutan penggabungan atom-atom yang menyusun molekul,
sedangkan stereoisomeri adalah isomeri dengan perbedaan terletak pada cara
penataan atom-atom dalam ruang, tetapi urutan penggabungan atom-atomnya tidak
berbeda. Sebagai contoh 1-butanol dan 2-butanol adalah isomer struktur,
karena urutan penggabungan atom oksigen dari gugus hidroksil (gugus OH) pada
rangka karbonnya berbeda. Akan tetapi, R-2-butanol dan S-2-butanol adalah dua
senyawa yang berstereoisomeri, keduanya mempunyai urutan penggabungan atom-atom
yang sama, tetapi penataan ruang atom-atom pada atom karbon nomor 2 tidak sama,
yang menyebabkan R-2-butanol dan S-2-butanol mempunyai sifat berbeda, yaitu
memutar bidang cahaya
terpolarisasi pada polarimeter ke arah yang berbeda.
Stereoisomeri merupakan peristiwa
terdapatnya beberapa senyawa berbeda dengan rumus molekul sama, dan perbedaan antara senyawa-senyawa tersebut
terletak pada cara penataan atom-atom dalam ruang, tetapi urutan penggabungan
atom-atomnya tidak berbeda. Terdapat berbagai jenis
stereoisomeri, yaitu isomeri geometri
(atau isomeri cis-trans),
dan isomeri konfigurasi.
Isomeri
Geometri
Isomeri geometri terdapat pada
senyawa-senyawa alkena yang pada setiap atom karbon ikatan rangkapnya mengikat
dua gugus yang berbeda. Isomeri
geometri didefinisikan sebagai peristiwa terdapatnya beberapa senyawa berbeda
yang mempunyai rumus molekul sama, dan perbedaan di antara senyawa-senyawa
tersebut terletak pada cara penataan gugus-gugus di sekitar ikatan rangkap.
Isomeri ini hanya ditemukan pada senyawa-senyawa yang berikatan tegar atau
rigid, sehingga tidak dapat berotasi, seperti alkena dan sikloalkana.
Isomeri geometri dapat terjadi
karena terdapat perbedaan penataan ruang gugus-gugus di sekitar ikatan rangkap
dua suatu alkena atau di sekitar dua karbon anggota cincin suatu sikloalkana.
Dua gugus yang terletak pada satu sisi yang sama, disebut cis (dari
Bahasa Latin, yang artinya pada sisi yang sama), sedangkan dua gugus yang
terletak pada sisi-sisi yang berlawanan disebut trans (dari Bahasa Latin, artinya bersebrangan).
Contoh isomeri
geometri adalah cis-1,2-dibromoetena dan trans-1,2- dibromoetena.
Keduanya merupakan dua senyawa berbeda, salah satunya dibuktikan dari perbedaan
titik didihnya. Urutan penggabungan atom-atom kedua senyawa tersebut sama,
tetapi penataan ruang atom-atom di sekitar ikatan rangkapnya berbeda, jadi
keduanya tidak termasuk isomeri struktur, tetapi stereoisomeri, khususnya
isomeri geometri. Perbedaan nama keduanya ditunjukkan dengan awalan cis dan
trans. Awalan cis digunakan untuk memberi nama alkena dengan dua
gugus pada kedua karbon berikatan rangkap terletak pada sisi yang sama.
Sebaliknya, awalan trans digunakan untuk memberi nama alkena dengan dua
gugus pada kedua karbon berikatan rangkap terletak pada sisi yang bersebrangan.
Persyaratan isomeri geometri adalah
tiap karbon yang terlibat dalam ikatan rangkap harus mengikat dua gugus yang
berlainan, misalnya H dan F, atau CH3 dan CH2CH3. Jika
salah satu karbon atau kedua karbon yang berikatan rangkap mengikat dua gugus
yang identik, misalnya dua atom Br atau dua gugus CH3, maka tak mungkin terjadi
isomeri geometri. Perhatikan bahwa pada contoh-contoh di bawah ini tidak
mungkin ditemukan isomeri geometri.
Isomeri geometri atau isomeri cis-trans
dapat ditemukan juga pada senyawa siklik berikatan tunggal atau
sikloalkana. Seperti juga pada ikatan rangkap, ikatan tunggal pada suatu
struktur cincin tidak dapat berotasi bebas. Oleh karena itu, bila terdapat dua
atom karbon anggota cincin yang masing-masing mengikat dua gugus berbeda selain
atom karbon anggota cincin, maka akan ditemukan isomeri geometri. Struktur cis,
bila gugus-gugus pada dua atom karbon cincin tersebut terletak pada sisi yang
sama dari bidang cincin, sebaliknya bila gugus-gugus pada dua atom karbon
cincin terletak pada sisi yang berlawanan dari bidang cincin, maka bentuk
struktur tersebut adalah trans.
Tampak pada cis-1,2-dikloroetana,
kedua gugus Cl terletak pada sisi yang sama dari ikatan rangkap. Bila kedua
gugus Cl berada pada posisi bersebrangan dari ikatan rangkap, maka terbentuk trans-1,2-dikloroetana.
Senyawa cis dan trans-1,2-dikloroetana merupakan dua senyawa yang
berbeda, seperti terlihat dari perbedaan titik didihnya.
Penamaan cis-trans pada
alkena dapat dilakukan bila pada kedua karbon berikatan tegar terdapat dua
gugus yang sama. Bila atom-atom karbon berikatan tegar mengikat empat gugus
yang berbeda, maka akan sulit untuk memberikan penamaan cis atau trans.
Perhatikan struktur di bawah ini, apakah merupakan struktur cis atau trans
?
Pada sistem seperti ini, tidak dapat
digunakan sistem penamaan cis-trans, akan tetapi harus digunakan sistem
penamaan yang lebih umum, yaitu sistem (E) dan (Z). Huruf E
berasal dari kata Bahasa Jerman “entgegen” yang berarti
bersebrangan, sedangkan huruf Z berasal dari kata Bahasa Jerman “zusammen”
yang artinya bersama-sama.
Sistem (E) dan (Z)
didasarkan pada pemberian prioritas kepada atom atau gugus yang terikat pada setiap
karbon ikatan rangkap. Jika kedua gugus berprioritas lebih tinggi terletak pada
sisi yang berlawanan, maka isomer itu adalah (E). Sebaliknya, bila kedua
gugus berprioritas tinggi terletak pada sisi yang sama, maka isomer iitu adalah
(Z). Secara sederhana ketentuan tersebut dapat dinyatakan dengan
Aturan
Penentuan Prioritas
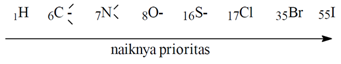
1. Prioritas
ditentukan oleh nomor atom dari atom yang berikatan langsung dengan atom-atom
karbon ikatan rangkap. Nomor atom yang lebih tinggi mempunyai prioritas yang lebih
tinggi.
2. Jika
atom-atom yang terikat sama, maka yang digunakan sebagai dasar adalah atom yang
terikat berikutnya sampai diperoleh perbedaan prioritas. Dalam contoh berikut
ditunjukkan nomor atom yang dijadikan dasar penentuan prioritas.
3. Atom-atom
yang terikat oleh ikatan rangkap dua atau rangkap tiga dianggap mengikat dua
atau tiga atom sejenis dengan ikatan tunggal. Tiap atom berikatan rangkap dua
didua-kalikan dan berikatan rangkap tiga, di tiga-kali-kan.
Perhatikan contoh sistem
penamaan alkena dengan sistem (E) dan (Z) berikut:
Isomeri
Konfigurasi
Jenis
stereoisomeri yang lain adalah isomeri konfigurasi atau isomer optis. Isomeri
konfigurasi terjadi pada molekul yang tidak mempunyai bidang simetri. Bidang
simetri adalah bidang imajiner yang membagi molekul menjadi dua bagian yang
satu sama lain adalah bayangan cerminnya. Molekul yang tidak mempunyai bidang
simetri akan berinteraksi dengan bidang cahaya terpolarisasi sehingga bidang
cahaya terpolarisasi akan berputar, baik ke kiri atau ke kanan. Kemampuan
memutar bidang cahaya terpolarisasi tersebut, baik arah maupun besar sudut
putarnya dapat diketahui dengan alat polarimeter. Salah satu ciri molekul yang
tidak mempunyai bidang simetri adalah pada molekul tersebut terdapat atom
karbon yang mengikat empat gugus berbeda. Atom karbon seperti itu disebut atom karbon kiral atau asimetris, yaitu
atom karbon yang mengikat 4 (empat) gugus berbeda. Cara penataan 4 (empat)
gugus berbeda pada suatu atom karbon kiral disebut konfigurasi. Oleh karena
itu, peristiwa terdapatnya beberapa senyawa berbeda yang mempunyai rumus
molekul sama, dan perbedaannya terletak pada konfigurasi atom karbon kiral
(penataan empat gugus berbeda di sekitar atom karbon kiral) disebut isomer konfigurasi.. Sebagai contoh,
atom karbon nomor 3 pada molekul 3-kloro-2-metilpentana adalah atom karbon
kiral, karena mengikat empat gugus berbeda, yaitu H, CH2CH3, Cl, dan CH(CH3)2.
Atom karbon kiral atau pusat kiral seringkali diberi tanda *. atom karbon kiral
atau asimetris.





















Assalamualaikim wahyuni andriani Saya akan menambahkan sedikit mengenai stereoisomer. Stereoisomer adalah molekul-molekul yang mempunyai rumus molekul dan konektivitas sama tetapi berbeda posisi atom-atom penyusunnya atau bentuk tiga dimensi susunannya. Stereoisomer adalah isomer karena atom mereka berbeda letak dari yang lain dalam hal penataan ruang (tiga dimensinya). Penataan ruang atom memperhatikan bagaimana partikel atom yang berbeda dengan molekul yang terletak di sekitar ruang dari senyawa organik, yaitu rantai karbon. Dalam hal ini, pengaturan tata ruang dari suatu molekul organik akan berbeda jika atom bergeser dalam arah tiga dimensi bahkan oleh satu derajat. Hal ini membuka kemungkinan yang sangat luas pada keberadaan molekul yang berbeda, masing-masing dengan penempatan atom yang unik dalam ruang tiga dimensi.
BalasHapusWaalaikumsalam tutut. Terimakasih atas penambahannya. Semoga bermanfaat bagi pembaca 😊
HapusAssalamu'alaikum yuni..
BalasHapusDari postingan diatas, saya ingin bertanya mengenai pernyataan isomeri geometri adalah isomeri yang disebabkan oleh perbedaan penataan ruang atom-atom dalam molekul. Isomeri jenis ini hanya terjadi pada senyawa yang memiliki ikatan yang kaku dengan dua sisi yang berlainan. Isomeri geometri hanya terjadi pada senyawa alkena. Mengapa hanya alkena? Mengapa alkana tidak? Jelaskan!
Terima kasih
Assalamu'alaikum yuni..
BalasHapusDari postingan diatas, saya ingin bertanya mengenai pernyataan isomeri geometri adalah isomeri yang disebabkan oleh perbedaan penataan ruang atom-atom dalam molekul. Isomeri jenis ini hanya terjadi pada senyawa yang memiliki ikatan yang kaku dengan dua sisi yang berlainan. Isomeri geometri hanya terjadi pada senyawa alkena. Mengapa hanya alkena? Mengapa alkana tidak? Jelaskan!
Terima kasih
Assalamu'alaikum yuni..
BalasHapusDari postingan diatas, saya ingin bertanya mengenai pernyataan isomeri geometri adalah isomeri yang disebabkan oleh perbedaan penataan ruang atom-atom dalam molekul. Isomeri jenis ini hanya terjadi pada senyawa yang memiliki ikatan yang kaku dengan dua sisi yang berlainan. Isomeri geometri hanya terjadi pada senyawa alkena. Mengapa hanya alkena? Mengapa alkana tidak? Jelaskan!
Terima kasih
Waalaikumsalam reni. Terimakasih atas pertanyaannya :)
HapusSaya akan mencoba menjawab.
Molekul di alam tidaklah diam atau statis, namun melakukan banyak gerakan, diantara gerakan yang paling umum adalah translasi (gerak lurus), rotasi (memutar), dan vibrasi (bergetar). Salah satu gerak yang akan kita tinjau adalah gerak rotasi. Pada senyawa alkana, dimana ikatan antar karbon adalah ikatan tunggal, maka molekul akan dapat berputar pada sumbunya dengan putaran yang bebas.
Perhatikan, kita ambil contoh senyawa butana (CH3-CH2-CH2-CH3 )
Kedua struktur diatas adalah struktur dari senyawa yang sama, meskipun gugus –CH3 sepertinya berlainan tempat, namun karena molekul dapat berputar, maka struktur tersebut dapat kembali ke struktur semula, dan ini dapat terjadi dalam waktu yang sangat cepat.
Adapun untuk senyawa yang mengandung ikatan rangkap (seperti alkena), ikatan rangkap tersebut akan bersifat kaku sehingga tidak dapat berputar. Nah, karena ikatan rangkap ini tidak dapat berputar, maka ketika ada dua senyawa yang memiliki struktur berbeda, itu artinya kedua senyawa tersebut memang merupakan dua senyawa yang berbeda sifat. Dengan kata lain, dua senyawa tersebut adalah isomer satu sama lain.
assalamualaikum, wahyuni tolong sebutkan penggolongan stereoisomer. Terimakasih
BalasHapusWaalaikumsalam sriwahyuni. Terimakasih atas pertanyaannya :)
HapusSaya akan mencoba menjawab
Berdasarkan strukturnya stereoisomer digolongkan menjadi dua yaitu :
1. Enantiomer adalah yang antara satu sama lain merupakan bayangan cermin
2. Diastereomer adalah yang bukan merupakan bayangan cermin, contohnya adalah isomer cis dan trans
Berdasarkan mudah tidaknya berubah dari satu stereoisomer ke stereoisomer yang lain, stereoisomer dikelompokan menjadi dua kelompok, yakni :
1. Isomer-isomer konformasi / konfomer-konfomer yaitu mereka yang dapat berubah dari satu stereoisomer ke stereoisomer yang lain dengan hanya melalui pemuatan ikatan tunggal
2. Isomer-isomer konfigurasi yaitu mereka yang hanya dapat berubah dari satu stereoisomer ke stereoisomer yang lain melalui pemutusan dan penyambungan kembali ikatan-ikatan kovalen.
boleh saya menanyakan bagaiman cara kita menentukan senyawa yang berisomer dan senyawa yang identik
BalasHapusapa perbedaan isometri cis-trans dengan isometri e-z?
BalasHapus